Two reasons why cancers thrive in chromosomal chaos
एक सना हुआ हिस्टोलॉजिकल स्लाइड, जिसे 100 गुना बढ़ाया गया है, कैंसर कोशिकाओं को सामान्य स्तन ऊतकों के माध्यम से फैलता है, जिसमें ट्यूमर कोशिकाओं से पूरी तरह से भरी हुई नलिका भी शामिल है। श्रेय: डॉ. सेसिल फॉक्स, राष्ट्रीय कैंसर संस्थान
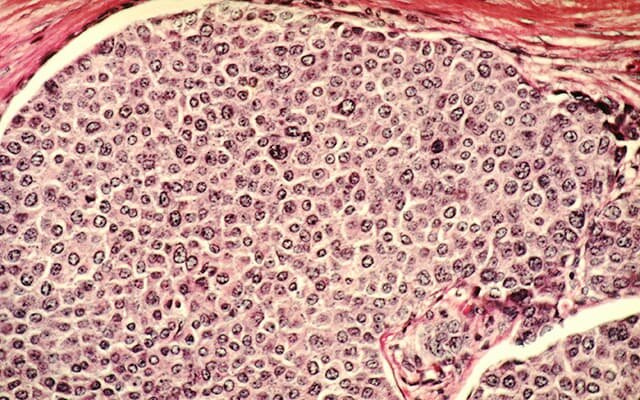 |
ईएमबीओ रिपोर्ट में लिखते हुए, यूसी सैन डिएगो हेल्थ में यूनिवर्सिटी ऑफ कैलिफोर्निया सैन डिएगो स्कूल ऑफ मेडिसिन और मूरेस कैंसर सेंटर के शोधकर्ताओं ने वर्णन किया है कि कैसे ट्यूमर के अस्तित्व और विकास को बढ़ावा देने के लिए कैंसर कोशिकाओं द्वारा मौलिक आनुवंशिक और सेलुलर प्रक्रियाओं की एक जोड़ी का शोषण किया जाता है।
निष्कर्ष पत्रिका के 26 अक्टूबर, 2021 के अंक में दिखाई देते हैं, जो यूरोपीय आणविक जीवविज्ञान संगठन का एक प्रकाशन है।
कैंसर कई प्रकार के आनुवंशिक परिवर्तनों से प्रेरित होता है, जिसमें डीएनए उत्परिवर्तन और प्रतिलिपि संख्या परिवर्तन छोटे सम्मिलन और विलोपन से लेकर पूरे जीनोम दोहराव की घटनाओं तक शामिल हैं।
सामूहिक रूप से, ट्यूमर में दैहिक प्रतिलिपि संख्या परिवर्तन के परिणामस्वरूप अक्सर गुणसूत्रों की एक असामान्य संख्या होती है, जिसे एयूप्लोइडी कहा जाता है, जिसे आनुवंशिक विविधता, अस्थिरता और विकास को बढ़ाकर ट्यूमर के विकास को बढ़ावा देने के लिए दिखाया गया है। लगभग 90 प्रतिशत ठोस ट्यूमर और आधे रक्त कैंसर किसी न किसी रूप में एयूप्लोइडी पेश करते हैं, जो ट्यूमर की प्रगति और खराब पूर्वानुमान से जुड़ा होता है।
हाल के वर्षों में, यह स्पष्ट हो गया है कि ट्यूमर माइक्रोएन्वायरमेंट के भीतर सहवास करने वाली कोशिकाएं न केवल बाहरी तनाव (मुख्य रूप से चयापचय मूल, जैसे पोषक तत्वों की कमी) के अधीन होती हैं, बल्कि आंतरिक तनाव aeuploidy के अधीन भी होती हैं। दोनों एक तनाव प्रतिक्रिया तंत्र को सक्रिय करते हैं जिसे अनफोल्डेड प्रोटीन रिस्पॉन्स (यूपीआर) कहा जाता है, जो कोशिकाओं के एंडोप्लाज्मिक रेटिकुलम (ईआर) में मिसफॉल्ड प्रोटीन के संचय की ओर जाता है - एक ऐसा अंग जो प्रोटीन को संश्लेषित करता है और उन्हें सेल के बाहर स्थानांतरित करता है।
जब यह प्राथमिक परिवहन/निर्यात प्रणाली बाधित हो जाती है, तो यूपीआर मिसफोल्डेड प्रोटीन के संचय को रोककर, उन्हें नीचा दिखाने और हटाने और उचित प्रोटीन फोल्डिंग को बढ़ावा देने के लिए सिग्नलिंग मार्ग को सक्रिय करके सामान्य कार्य को बहाल करने का प्रयास करता है।
यदि होमोस्टैसिस या संतुलन जल्दी से फिर से स्थापित नहीं होता है, तो गैर-ट्यूमर कोशिकाएं कोशिका मृत्यु से गुजरती हैं। इसके विपरीत, कैंसर कोशिकाएं इस अराजकता में पनपती हैं, एक उच्च सहिष्णुता सीमा स्थापित करती हैं जो उनके अस्तित्व का पक्ष लेती हैं।
यूसी सैन डिएगो स्कूल ऑफ मेडिसिन में मेडिसिन के प्रोफेसर सह-वरिष्ठ लेखक मौरिजियो ज़ानेटी ने कहा, "इन परिस्थितियों में, वे धोखे के एक सर्पिल में पड़ोसी कोशिकाओं को भी सह-चयन करते हैं जो उत्तरोत्तर स्थानीय प्रतिरक्षा कोशिकाओं को खराब करता है।" हन्ना कार्टर, पीएच.डी., मेडिसिन के एसोसिएट प्रोफेसर और एक कम्प्यूटेशनल बायोलॉजिस्ट के साथ मूरेस कैंसर सेंटर। ज़ानेटी ने पहले एक विज्ञान टिप्पणी में परिकल्पना पेश की थी।
शोधकर्ताओं ने अनुमान लगाया कि aeuploidy, UPR और प्रतिरक्षा कोशिका विकृति को एक घातक त्रिकोण में एक साथ जोड़ा जा सकता है। नए अध्ययन में, ज़ानेटी, कार्टर और उनके सहयोगियों ने 9,375 मानव ट्यूमर के नमूनों का विश्लेषण किया और पाया कि कैंसर कोशिका aeuploidy तनाव के लिए संकेतन प्रतिक्रिया की कुछ शाखाओं के साथ अधिमानतः प्रतिच्छेद करती है और यह खोज टी लिम्फोसाइटों पर aeuploidy के हानिकारक प्रभावों से संबंधित है, एक प्रकार का प्रतिरक्षा कोशिका।
"यह एक महत्वाकांक्षी लक्ष्य था जिसका पहले प्रयास नहीं किया गया था," ज़ानेटी ने कहा। "यह तीन मुख्य प्रणालियों से एक साथ पूछताछ करने जैसा था - पूर्ण रूप से गुणसूत्र संबंधी असामान्यताएं, अंतर्जात तनाव और पड़ोसी प्रतिरक्षा कोशिकाओं के अपचयन के जवाब में सिग्नलिंग तंत्र - बस एक साहसिक परिकल्पना साबित करने के लिए।"
"हम जानते थे कि कार्य चुनौतीपूर्ण होगा," कार्टर ने कहा, "और हमें विषम मानव ट्यूमर डेटा में अपनी परिकल्पनाओं का परीक्षण करने के लिए नए विश्लेषणात्मक उपकरण बनाने और परिष्कृत करने की आवश्यकता होगी, लेकिन यह एक सार्थक जोखिम था।"
उन्होंने कहा, निष्कर्ष बताते हैं कि कैंसर कोशिकाओं में तनाव प्रतिक्रिया "प्रतिरक्षा क्षमता और एंटी-ट्यूमर प्रभाव को कम करने" के लिए aeuploidy और प्रतिरक्षा कोशिकाओं के बीच एक अप्रत्याशित कड़ी के रूप में कार्य करती है। यह यह भी दर्शाता है कि एन्युप्लोइड कोशिकाओं द्वारा जारी अणु एक अन्य प्रकार की प्रतिरक्षा कोशिकाओं को प्रभावित करते हैं - मैक्रोफेज - उनके सामान्य कार्य को बदलकर उन्हें ट्यूमर को बढ़ावा देने वाले अभिनेताओं में बदल देते हैं।
लेखकों ने कहा, निष्कर्ष ट्यूमर की प्रगति को ट्यूमर के विकास के दौरान गुणसूत्र असामान्यताओं के प्रगतिशील संचय और एंटी-ट्यूमर प्रतिरक्षा के प्रगतिशील क्षय के बीच संतुलन के रूप में समझने के नए अवसर प्रदान करते हैं, लेखकों ने तनाव गेजिंग और रिश्ते को विनियमित करने के लिए सिग्नलिंग प्रतिक्रिया के साथ कहा।
व्यावहारिक रूप से, उन्होंने कहा, अध्ययन के लिए विकसित क्रोमोसोमल असामान्यताओं के बोझ को परिभाषित करने वाला एक नया एयूप्लोइडी स्कोर, रोगियों में ट्यूमर की प्रगति के जैविक चरण का आकलन करने के लिए एक नया प्रतिमान स्थापित कर सकता है और प्रतिरक्षा स्थिति को बाहर निकालने के लिए उपयोग किया जा सकता है।
"यह औषधीय या आनुवंशिक हस्तक्षेपों के लिए नए अवसरों के बारे में भी सूचित कर सकता हैयूपीआर की विशिष्ट शाखाओं के साथ हस्तक्षेप करने के लिए aeuploidy- संचालित स्थानीय प्रतिरक्षा विकृति के मध्यस्थ के रूप में। यह गैर-इम्यूनोलॉजिकल दृष्टिकोण कैंसर की इम्यूनोथेरेपी को और अधिक कुशल बना सकता है," ज़ानेटी ने कहा।
सह-लेखकों में शामिल हैं: सु जियान, मैगली डोसेट, गोंजालो अल्मांज़ा, स्टीफन सियरल्स, पारस साहनी, टी। कैमरन वालर, क्रिस्टन जेपसेन और हन्ना कार्टर, सभी यूसी सैन डिएगो में।




